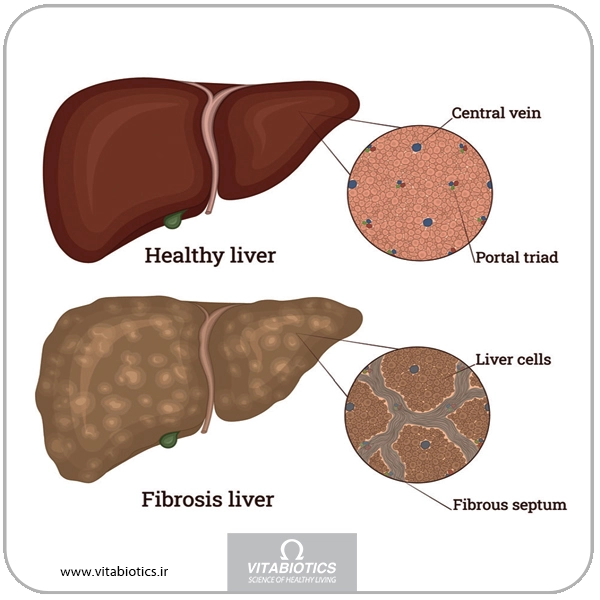
فیبروز کبدی یک بیماری مزمن کبدی است که در اثر بر هم خوردن تعادل ماتریکس خارج سلولی و تخریب بافت کبدی به وجود میآید. این بیماری مرگ و میر بالایی دارد اما تا به امروز داروی مناسبی برای آن کشف نشده است.
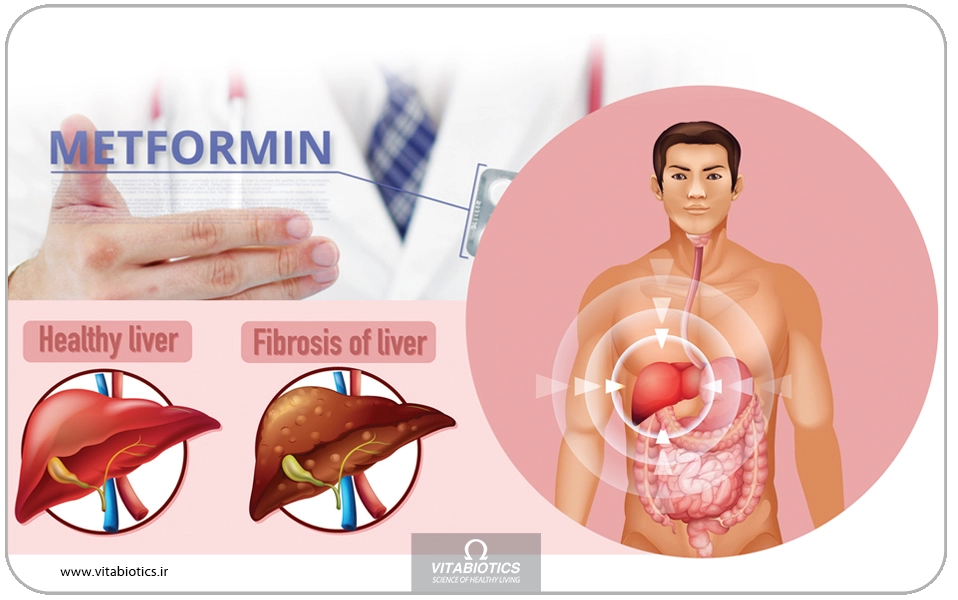
درصورتی که بیمار تحت درمان قرار نگیرد ممکن است که بیماری شدت پیدا کند و به سیروز کبدی، سرطان کبدی یا نارسایی کبدی منجر شود. متفورمین دارویی است که گلوکز خون را کاهش میدهد و درعینحال آثار ضدالتهابی دارد. طی آزمایشهای گوناگون روی سلولهای زنده و حیوانات مشخص شده است که متفورمین روی فیبروز کبدی تأثیر مثبتی میگذارد اما مکانیسم آن هنوز نامشخص است. در این مقاله مروری پس از معرفی فیبروز کبدی به برخی از تئوریهای مطرح شده برای مکانیسم اثر متفورمین روی فیبروز کبدی و آثار احتمالی آن میپردازیم.
علت فیبروز کبدی
دلایل به وجود آمدن فیبروز کبدی گوناگون است و از جمله آنها میتوان به هپاتیت B و C، تخریب بافت کبدی در اثر دارو، الکل یا کبد چرب غیرالکلی اشاره کرد. کبد چرب غیرالکلی به عنوان اصلیترین علت اختلالات کبدی مزمن و فیبروز کبدی در نظر گرفته میشود. آسیب به کبد منجر به فعال شدن سلولهای ستارهای کبدی (HSC) میشود که خود به میوفیبروبلاست تبدیل میشوند و ترشح ماتریکس خارج سلولی را افزایش میدهند. مقادیر بالای ماتریکس خارج سلولی منجر به فیبروز کبدی میشود. تحقیقات نشان میدهند که هپاتوسیتها، سلولهای مجرای صفرا، سلولهای ستارهای کبدی، سلولهای اندوتلیال کبدی و سلولهای دستگاه ایمنی به ویژه ماکروفاژها در به وجود آمدن فیبروز کبدی نقش دارند. کاربرد اصلی متفورمین کاهش قند خون است که از طریق افزایش جذب گلوکز توسط سلولها و مهار ر گلیکوژنز در کبد این کار را انجام میدهد.
متفورمین همچنین برای کاهش احتمال ابتلا به بیماریهای قلبی-عروقی، سرطان کولون و مقعد، سندروم تخمدان پلیکیستیک به کار میرود. از آثار دیگر متفورمین میتوان به خاصیت ضد توموری آن و نقش آن در کاهش شدت فیبروز کبدی در بیماران مبتلا به دیابت شیرین نوع 2 اشاره کرد. دیابت شیرین نوع 2 یکی از ریسک فاکتورهای مهم فیبروز کبدی به ویژه در بیماران مبتلا به کبد چرب میباشد. طبق آمار تخمینی 21 درصد مبتلایان به دیابت شیرین نوع 2 فیبروز کبدی دارند.
همچنین تحقیقات دیگر نشانگر این است که پس از 2 سال مصرف متفورمین در 57.8 درصد از بیماران مبتلا به دیابت شیرین نوع 2 کاهش شدت فیبروز کبدی مشاهده شده است.
مکانیسم های اثر متفورمین بر فیبروز کبدی:
تحقیقات نشان میدهند که سلولهای کوپفر، سلولهای مجرای صفرا و سلولهای ستارهای کبدی، سلولهای میوفیبروبلاست ستارهای کبدی 2 را تحریک میکنند تا پروتئینهای خارج سلو
لی زیادی ترشح کنند و همچنین عواملی مانند فاکتور رشد تغییردهنده 3 و فاکتور رشد مشتق از پلاکت 4 که خود تشدیدکننده فیبروز هستند را افزایش دهند. در صورت آسیب کبدی، سلولهای ستارهای به میوفیبروبلاستها تبدیل میشوند.
مکانیسم 1: متفورمین و سلولهای ستارهای کبدی
سلولهای ستارهای اصلیترین سلولهای دخیل در فیبروز کبدی هستند. این سلولها در فرم میوفیبروبلاستیک خود ماتریکس خارج سلولی زیادی ترشح میکنند که باعث تخریب کبد و فیبروز میشود. در نتیجه مهار فعال شدن سلولهای ستارهای، فیبروز را کاهش میدهد. متفورمین آگونیست پروتئین کیناز فعال شده توسط آدنوزین مونوفسفات (AMPK) است و با افزایش پروتئین کیناز در سلولهای غیرمیوفیبروبلاستیک باعث مهار فعال شدن سلولهای ستارهای میشود.
از سوی دیگر، متفورمین باعث آپوپوتوز در سلولهای ستارهای فعال شده میشود. فاکتور رشد تغییردهنده بتا (TGF-ß) در تبدیل سلولهای ستارهای به میوفیبروبلاستها نقش دارد و متفورمین آن را کاهش میدهد. تبدیل سلول ستارهای به میوفیبروبلاست همچنین انرژی زیادی میخواهد که این انرژی از طریق زنجیره انتقال الکترون در میتوکندری تولید میشود و متفورمین باعث مهار این زنجیره میشود.
مکانیسم 2: متفورمین و سـلول های کوپفرکوپفرها
متفورمین و سـلول های کوپفرکوپفرها ماکروفاژهای باقیمانده در کبد میباشند و نقش آنها در پاسخ التهابی و فیبروز در اثر آسیب کبدی ثابت شده است. متفورمین از طریق فعال کردن AMPK تبدیل مونوسیت به ماکروفاژ را مختل میکند، اما مکانیسم این عمل هنوز مشخص نشده است. کوپفرها ترشح ß-TGF و همچنین فیبرین بین سلولی را افزایش میدهند و باعث میشوند که ماتریکس بین سلولی بیشتری تولید شود و فیبروز شدت پیدا کند. البته سلولهای کوپفر به دو دسته M1 و M2 تقسیم میشوند که M1 خواص التهابی از خود نشان میدهد و ترشح سایتوکاینهای التهابی را افزایش میدهد اما M2 خواص ضدالتهابی دارد و سایتوکاینهای ضدالتهابی ترشح میکند. متفورمین تولید ماکروفاژهای M1 کبدی را کاهش میدهد و از سوی دیگر تعداد ماکروفاژهای M2 را افزایش میدهد.
مکانیسم 3: متفورمین در هپاتوسیتها
آسیب به هپاتوسیتها در اثر الکل، عفونتهای ویروسی و مواد سمی باعث میشود که این سلولها عوامل التهابی مانند گونههای فعال اکسیژن (ROS) تولید کنند. ROS در نهایت منجر به آسیب به DNA و آپوپتوز هپاتوسیتها میشود. آپوپتوز سلولهای میوفیبروبلاستی ستارهای را فعال میکند و به فیبروز منتهی میشود. متفورمین تولید ROS را کاهش میدهد و به بقای سلولی کمک میکند. لیزوفسفاتیدیل کولین (LPC) منجر به تبدیل لیپید به لیپوهپاتیت و در نهایت آپوپتوز میشود. متفورمین حساسیت به انسولین را افزایش میدهد و درصد LPC در سلولهای کبدی را کاهش میدهد.
مکانیسم 4: متفورمین و سلولهای مجرای صفرا
سلولهای مجرای صفرا داخل و خارج کبد یافت میشوند. این سلولها باعث فیبروز، التهاب و اختلال کبدی و به دنبال آن اختلال در ترشح صفرا میشوند. سلولهای مجرای صفرا همچنین میتوانند باعث فعال شدن سلولهای ستارهای و افزایش ماتریکس خارج سلولی شوند. اختلال در تنظیم مولکول هدف راپامایسین در پستانداران (mTOR) باعث افزایش تکثیر سلولی می شود. متفورمین مسیر mTOR/AMPK را فعال میکند و از تکثیر زیاد سلولهای مجرای صفرا درون کبدی و سرطانی شدن آنها جلوگیری میکند و فیبرهای کلاژن را کاهش میدهد. مطالعات درونسلولی همچنین نشان میدهد که متفورمین با هدف قرار دادن NF-ƙB از تکثیر بیش از حد سلولهای مجرای صفرا جلوگیری میکند.
مکانیسم 5: متفورمین و سلولهای سینوزوئیدی اندوتلیال
رگزایی گام مهمی در بازسازی کبد پس از آسیب است. سلولهای ستارهای کبدی و سلولهای سینوزوئیدی اندوتلیال در رگزایی نقش اصلی را بر عهده دارند. سلولهای سینوزوئیدی اندوتلیال برخلاف سلولهای عمومی اندوتلیال دیواره عروق، سلولهای تخصصی اندوتلیال محسوب میشوند. آنژیوزنز سایتوکاین های مختص خود را تولید میکند، مانند عامل رشد اندوتلیال عروقی (VEGF،VGEF2).
از سوی دیگر، سلولهای سینوزوئیدی اندوتلیال ممکن است به صورت فیزیکی به سلولهای ستارهای فشار بیاورند و از این طریق آنها را فعال کنند که در نهایت هر دو حالت به فیبروز کبدی منتهی میشود. متفورمین میتواند بیان VEGF را کاهش دهد و رگزایی ناشی از سلولهای ستارهای را مهار کند. در نهایت لازم به ذکر است که تمامی تحقیقات انجامشده از نوع گذشتهنگر بودهاند و هنوز مطالعه کنترلشده تصادفی (Randomized Controlled Trial) مناسبی در زمینه بررسی اثر متفورمین بر فیبروز کبدی انجام نشده است. بنابراین، باوجود اینکه متفورمین آثار قابل توجهی روی کنترل فیبروز کبدی نشان داده است، مکانیسم عمل آن همچنان ناشناخته باقی میماند.
نکته دیگری که باید به آن توجه شود این است که آزمایشهای انجامشده بیشتر روی موشها صورت گرفتهاند و به دلیل تفاوت میان انسان و موش، نتایج ممکن است در برخی موارد قابل تعمیم نباشند.